مرجع پلیمر در بازار ایران (پلیم پارت) :
استراتژیهای مرسوم و در حال ظهور برای ساخت و عملکرد دستگاههای میکروسیال مبتنیبر PDMS
چکیده
میکروسیالها زمینهای نوظهور و چند رشتهای هستند که مورد توجه تولیدکنندگان در پزشکی، بیوتکنولوژی و شیمی قرار گرفتهاند؛ زیرا ابزارهای منحصربهفردی را برای توسعه تشخیصهای نقطهای مراقبت، سیستمهای اندام روی تراشه و حسگرهای زیستی فراهم مینمایند. میکروسیالهای پلیمری، بر خلاف شیشه و سیلیکون، مزایای متعددی مانند تولید انبوه کمهزینه و طیف گستردهای از خواص مفید مواد را ارائه میدهند که آنها را به ماده انتخابی برای کاربردهای تجاری و سیستمهای با توان بالا تبدیل مینماید. در میان پلیمرهای مورد استفاده برای ساخت دستگاههای میکروسیال، پلیدیمتیل سیلوکسان (PDMS) به دلیل ویژگیهای سودمند آن، مانند شفافیت عالی و زیستسازگاری، از جمله پرمصرفترین و پرکاربردترین ماده در دانشگاهها میباشد. با این حال، تجاریسازی PDMS بیشتر به دلیل هزینه بالا در استراتژیهای ساخت فعلی چالش برانگیز بوده است. علاوهبر این، مراحل خاص اصلاح سطح و عاملسازی برای تنظیم شیمی سطح کانالهای PDMS مانند تثبیت مولکولهای زیستی، آبگریزی سطح و خواص ضد رسوب با توجه به کاربرد نهایی مورد نیاز میباشد. در حالی که تحقیقات قابل توجهی در زمینه میکروسیالات PDMS گزارش شده است، عملکرد سطوح PDMS مرحلهای حیاتی در فرآیند ساخت است که هدایت آن دشوار میباشد. در این پژوهش ابتدا تصویر کاملی از روشهای ساخت موجود برای دستگاههای میکروسیال مبتنیبر PDMS ارائه میشود که چندین پیشرفت اخیر در این زمینه با هدف کاهش هزینه و زمان برای تولید انبوه این دستگاهها را ارائه میدهد. در مرحله بعد، روشهای مختلف مرسوم و نوظهور برای مهندسی شیمی سطح PDMS به تفصیل مورد بحث قرار میگیرند. طیف گستردهای از تکنیکهای عاملسازی در ادامه ارائه میشود که ریزکانالهای PDMS را برای ثبات فیزیکی یا کووالانسی موجودات بیولوژیکی مختلف و در عین حال از فعل و انفعالات غیر اختصاصی بسیار سازگار مینماید.
نتیجهگیری و چشمانداز آینده
روشهای کمهزینه جدید برای ساخت میکروسیالهای PDMS و معرفی رابطهای عملکردی در کانالها، از طریق کوچکسازی و سادهسازی دستگاههای درمانی و تشخیصی فعلی، پیشرفت عظیمی را در اجرای این دستگاهها برای کاربردهای پزشکی و سیستمهای زیستتحلیلی ایجاد مینماید.
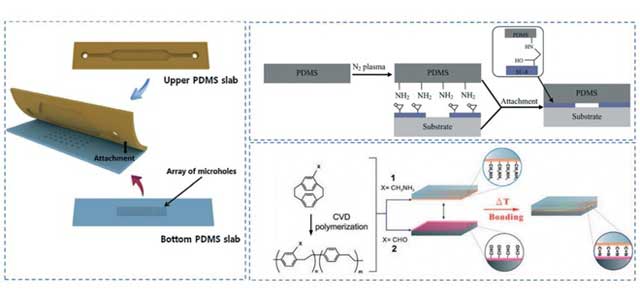
لیتوگرافی نرم PDMS با استفاده از قالبهای اصلی سیلیکونی و به دنبال آن پیوند پلاسمای اکسیژن امیدوارکنندهترین رویکرد گزارش شده در پژوهشهای پیشین برای ساخت میکروسیالات PDMS است. قالبهای اصلی به طور معمول از طریق تکنیکهای فتولیتوگرافی ساخته میشوند. با این حال، هزینه بالای امکانات و زمانبر بودن ساخت فرآیندی، فرصتهای بزرگسازی و تجاریسازی میکروسیالهای PDMS را مختل مینماید. همانطور که در این پژوهش بحث و بررسی میشود، استفاده از نور LED قابل حمل به جای لامپهای جیوهای ولتاژ بالا و همچنین لاک ناخن MA به جای SU-8 میتواند هزینه ساخت را کاهش دهد. علاوه بر این، روشهای بدون ماسک مانند نوشتن مستقیم لیزر، پرتو الکترونی و پرتو یون متمرکز، پلیمریزاسیون دو فوتونی و آینههای میکرو دیجیتال میتوانند باعث کاهش هزینههای ساخت شوند. استراتژیهای دیگری مانند لمینیت فیلمهای خشک ADEX، تکنیکهای پرینت سهبعدی با مرحله فلوئوروسیلانیزاسیون بیشتر و فرسایش لیزری یا ریزماشینکاری زیرلایههای PMMA میتواند نیاز به محیط اتاق تمیز را برطرف نماید. همچنین امکان تشکیل مستقیم میکروکانالها در دالهای PDMS با استفاده از پرتو الکترونی کم انرژی یا لیزر CO2 توضیح داده میشود که مراحل ساخت قالب اصلی را حذف مینماید. به عنوان جایگزین برای درمان پلاسما، روشهای مقرونبهصرفهتری مانند PDMS خشک نشده یا نیمه پختشده، فیلمهای چسبنده و قابل پخت با شعله میتوانند برای اتصال PDMS و محصور نمودن دستگاه استفاده شوند. علاوه بر این، تابش پرتو الکترونی یا پرتوهای![]() امکان پیوند همزمان دستهای از لایههای PDMS که قبلاً روی هم قرار گرفتهاند را میدهد، که برای تولید دستهای میکروسیالهای سهبعدی مفید است. این جایگزینهای ساخت فتولیتوگرافی میتواند زمان و هزینه مورد نیاز برای تولید انبوه میکروسیالهای PDMS را به میزان قابل توجهی کاهش دهد و به تجاریسازی این دستگاهها کمک نماید. با این وجود، به دلیل برخی محدودیتهای مرتبط با استراتژیهای جایگزین، مانند عدم وضوح و دقت مناسب برای کانالهای تولید شده و سرعت پایین ذاتی رویکردهای بدون ماسک، اجرای این استراتژیها برای افزایش مقیاس هنوز کاملاً چالش برانگیز است و جا برای این کار و پیشرفتهای بیشتر در این زمینه وجود دارد. جالب توجه است که در پروتکلی که توسط Bhattacharjee و همکاران آن ارائه شده است، کل میکروکانالهای PDMS با استفاده از چاپگر استریولیتوگرافی رومیزی به صورت سهبعدی چاپ میشوند. آنها از ماکرومرهای -PDMSمتاکریلات به عنوان رزین برای چاپ سهبعدی استفاده مینمایند و پس از استخراج ترکیبات واکنش نداده با استفاده از حلالهای مختلف موفق به دستیابی به کانالهای شفاف PDMS مناسب برای کشت سلولی میشوند. گونزالس و همکاران آن همچنین با استفاده از فرمولی مبتنیبر PDMS آکریلات، میکروکانالی شبیه PDMS را از طریق چاپ پردازش نور دیجیتال (DLP) چاپ نموند. با وجود تمام این محدودیتها، PDMS همچنان به عنوان جذابترین انتخاب برای نمونهسازی دستگاههای میکروسیال برای تحقیق و توسعه باقیمانده است.
امکان پیوند همزمان دستهای از لایههای PDMS که قبلاً روی هم قرار گرفتهاند را میدهد، که برای تولید دستهای میکروسیالهای سهبعدی مفید است. این جایگزینهای ساخت فتولیتوگرافی میتواند زمان و هزینه مورد نیاز برای تولید انبوه میکروسیالهای PDMS را به میزان قابل توجهی کاهش دهد و به تجاریسازی این دستگاهها کمک نماید. با این وجود، به دلیل برخی محدودیتهای مرتبط با استراتژیهای جایگزین، مانند عدم وضوح و دقت مناسب برای کانالهای تولید شده و سرعت پایین ذاتی رویکردهای بدون ماسک، اجرای این استراتژیها برای افزایش مقیاس هنوز کاملاً چالش برانگیز است و جا برای این کار و پیشرفتهای بیشتر در این زمینه وجود دارد. جالب توجه است که در پروتکلی که توسط Bhattacharjee و همکاران آن ارائه شده است، کل میکروکانالهای PDMS با استفاده از چاپگر استریولیتوگرافی رومیزی به صورت سهبعدی چاپ میشوند. آنها از ماکرومرهای -PDMSمتاکریلات به عنوان رزین برای چاپ سهبعدی استفاده مینمایند و پس از استخراج ترکیبات واکنش نداده با استفاده از حلالهای مختلف موفق به دستیابی به کانالهای شفاف PDMS مناسب برای کشت سلولی میشوند. گونزالس و همکاران آن همچنین با استفاده از فرمولی مبتنیبر PDMS آکریلات، میکروکانالی شبیه PDMS را از طریق چاپ پردازش نور دیجیتال (DLP) چاپ نموند. با وجود تمام این محدودیتها، PDMS همچنان به عنوان جذابترین انتخاب برای نمونهسازی دستگاههای میکروسیال برای تحقیق و توسعه باقیمانده است.
با توجه به عملکرد میکروکانالهای مبتنیبر PDMS، پلیمریزاسیون پیوندی به عنوان بهترین روش برای دستیابی به خواص آبدوستی و ضد رسوب طولانی مدت در میکروسیالات PDMS ثابت شده است. در کار گونزالس و همکاران آن، از آنجایی که هنوز پیوندهای دوگانه آکریلیک واکنش نداده پس از مرحله چاپ سهبعدی وجود داشت، میتوانستند گروههای کربوکسیلیک را با استفاده از اسید اکریلیک از طریق روش پلیمریزاسیون “پیوندخوردگی بر” تحت نور UV بر روی سطح القا نمایند. آنها همچنین امکان الگوبرداری از مناطق آبگریز/آبدوست در داخل کانالهای میکروسیال را با استفاده از محلول پیوند در ترکیب با روغن سیلیکون نشان میدهند.
عملآوری آمینی این سیستمهای میکروسیال با استفاده از سیلانیزاسیون APTES یا پیوند پلیمرهای پایانیافته آمینی یکی از موثرترین استراتژیها برای تثبیت کووالانسی مولکول های زیستی است. گروههای آمین اولیه میتوانند به صورت کووالانسی به چندین موجودیت عملکردی مانند گروههای اپوکسی، آلدهیدی و کربوکسیلیک (از طریق شیمی کربودیایمید) متصل شوند.
پیشنهاد برای تولید گروههای عاملی در کانالهای میکروسیال، استفاده از تصفیه پلاسمای CO2 به عنوان رویکرد اصلاح سطح، ساده و سریع است. بستر شیشهای تصفیهشده با پلاسما CO2 میتواند به طور برگشتناپذیری به پلتفرم PDMS متصل شود تا میکروکانال را تشکیل دهد. علاوه بر این، گروههای کربوکسیلیک میتوانند در داخل کانال برای فعالسازی بیشتر از طریق شیمی EDC-NHS به منظور تثبیت کووالانسی مولکولهای زیستی، فعال باقی بمانند. این کار نیاز به عاملدار نمودن سطح را از طریق روشهای شیمی مرطوب (مانند عملآوریAPTES/APTMS ) قبل از تثبیت بیومولکول حذف مینماید. همچنین میتوان به صورت کووالانسی کانالهای PDMS را توسط مولکولهای زیستی با استفاده از چاپ میکروکنتاکت الگوبرداری نمود. این استراتژی به طور بالقوه میتواند برای ایجاد رابطهای زیستی قوی در کانالهای میکروسیال پلیمری به روشی ساده تنظیم شود.
لین و همکاران آن به طور جالبی پیشنهاد ریختهگری PDMS روی پوست خشک شده کوسه برای دستیابی به خواص فوقآبگریزی را پیشنهاد نمودند. در طراحی آنها، پس از ریختهگری و تولید قالب منفی PDMS، قالب با پوشش پلاتین و برای اجرای دیگری از ریختهگری PDMS استفاده شد تا در نهایت برآمدگیهای پوست کوسه روی PDMS تکرار شود. غشای PDMS فوقآبگریز نهایی توانست به طور موثری در برابر اتصال باکتری مقاومت نماید. آنها همچنین با پوشاندن غشای PDMS با PVA و ![]() لایهی PDMS فوقآبدوست تولید نمودند. ترکیبی از دو لایه فوقآبگریز/آبدوست برای کاربردهای ترمیم زخم برای سرکوب همزمان چسبندگی باکتری و جذب ترشحات زخم استفاده میشود، در حالی که MPC میتواند ترمیم زخم را افزایش دهد. اگرچه آنها از این سیستم برای میکروسیالها استفاده ننمودند، اما این تکنیک میتواند با کاربردهای میکروسیال در جایی که آبگریز بودن برای دفع باکتریها مورد نیاز است، ادغام شود. در مطالعه دیگری، Poly(N-vinylpyrrolidone) (PVP) روی بستر PDMS عملآوری شده با آمین پوشش داده میشود تا زاویه تماس PDMS از 116 به 14 کاهش یابد. PVP در ابتدا با کتکول عاملدار میشود تا بتواند از طریق واکنش با گروههای آمینی PDMS به PDMS چسبیده شود. اجرای این استراتژی در میکروسیالها میتواند سودمند باشد زیرا میتواند میزان جذب آبگریزی پروتئینها را کاهش دهد.
لایهی PDMS فوقآبدوست تولید نمودند. ترکیبی از دو لایه فوقآبگریز/آبدوست برای کاربردهای ترمیم زخم برای سرکوب همزمان چسبندگی باکتری و جذب ترشحات زخم استفاده میشود، در حالی که MPC میتواند ترمیم زخم را افزایش دهد. اگرچه آنها از این سیستم برای میکروسیالها استفاده ننمودند، اما این تکنیک میتواند با کاربردهای میکروسیال در جایی که آبگریز بودن برای دفع باکتریها مورد نیاز است، ادغام شود. در مطالعه دیگری، Poly(N-vinylpyrrolidone) (PVP) روی بستر PDMS عملآوری شده با آمین پوشش داده میشود تا زاویه تماس PDMS از 116 به 14 کاهش یابد. PVP در ابتدا با کتکول عاملدار میشود تا بتواند از طریق واکنش با گروههای آمینی PDMS به PDMS چسبیده شود. اجرای این استراتژی در میکروسیالها میتواند سودمند باشد زیرا میتواند میزان جذب آبگریزی پروتئینها را کاهش دهد.
به منظور افزایش ویژگی رابطهای زیستی ایجاد شده، فناوری سطح تزریق شده با روانکننده میتواند کاندیدی امیدوارکننده برای دفع موثر انواع جذب غیراختصاصی باشد، در نتیجه حساسیت و کارایی دستگاههای میکروسیال را افزایش میدهد. نشان داده میشود که ترکیب سطوح تزریقشده با روانکننده با استراتژیهای ریزالگوسازی در میکروسیالها با بسترهای شیشهای میتواند منجر به ایجاد رابطهای زیستی موضعی با حساسیت بالا در جذب آنتیبادیها یا سلولهای ثانویه شود. ادغام این پروتکل با میکروسیالهای PDMS میتواند حسگرهای زیستی انعطافپذیر با حساسیت بالا به دلیل وجود روانکننده ایجاد نماید.
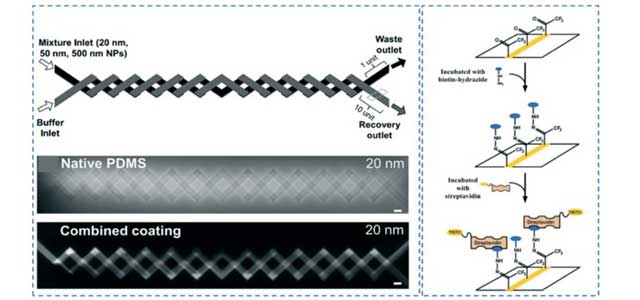
همچنین میتوان از طریق پوشش کانالها با نانوذرات طلا(AuNPs) به افزایش حساسیت زیستی روی پلتفرمهای میکروسیال PDMS دست یافت. AuNPها میتوانند به سادگی با آنتیبادیهای جذب یا سایر مولکولهای زیستی از طریق واکنش تیول با استفاده از پیوندهای متقاطع مانند MPTMS یا زیست مولکولهای کونژوگه با تیول فعال شوند. بنابراین، آنها سطح قابل توجهی از بزرگی را برای تشخیص مولکولهای زیستی هدف فراهم مینمایند. زو و همکاران تثبیت AuNPها را روی PDMS عملآوری شده با آمین نشان میدهند، که متعاقباً با آپتامرهای پایانیافته تیولی استافیلوکوکوس اورئوس (S. aureus) کونژوگه میشوند تا استافیلوکوکوس اورئوس را از طریق پراکندگی رامان تقویتشده سطحی(SERS) شناسایی نمایند. استفاده از این تکنیک عاملسازی سطحی برای میکروسیالهای PDMS به طور بالقوه میتواند حد تشخیص را افزایش دهد.
اخیراً بانرجی و همکاران هیدروژل PDMS خود ترمیم شونده با قابلیت ضد رسوب با استفاده از پلیمرزومهای PDMS zwitteronic و پلیمرزومهای PDMS عاملدار آمینی ارائه نموند. آنها داروی کورکومین را برای کاربردهای درمانی برای بیماریهای چشمی در هیدروژل به دام انداختند. خواص خود ترمیم شوندگی و ضد رسوب هیدروژل مبتنیبر PDMS برای میکروکانالهای PDMS با ماندگاری بالا، اگر بتوان این فناوری را در میکروسیالها گنجاند، بسیار مفید است. علاوه بر این، لامرز و همکاران آن موفق به دستیابی به خواص مکانیکی مختلفی از PDMS (از PDMS چسبناک تا PDMS شکننده) از طریق عاملدار نمودن پیکره PDMS با hydz، بنزن-1،3،5-کربوکسامید(BTA)و یوریدوپیریمیدینون (UPy) شدند. آنها همچنین قابلیت بازیافت PDMSهای اصلاح شده را از طریق حلالسازی، قالبگیری فشرده یا بازیافت حرارتی نشان دادند. این قابلیت، اگر در میکروسیالها تعبیه شود، میتواند نسل جدیدی از میکروکانالهای PDMS قابل بازیافت سازگار با محیطزیست را ایجاد نماید.
علاوه بر این، الگوبرداری از مولکولهای زیستی در کانالهای میکروسیال PDMS امکان تشخیص چندگانه بیومارکرهای مختلف را برای کاربردهای با توان بالا فراهم مینماید. ترکیب روشهای ساده مانند چاپ میکروکنتاکت از طریق استفاده از مهرهای PDMS با ساخت میکروسیال میتواند روشی را در مقایسه با سایر تکنیکهای الگوسازی مانند چاپ بدون تماس با فناوری چاپ جوهرافشان پیزوالکتریک، الگوبرداری فوتولیتوگرافی با استفاده از ماسک نوری مناسب و طرحهای چند وجهی به شکل درخت برای تولید شیب غلظت دو بعدی (2D) سادهتر نماید. با بهرهگیری از مقاومتهای هیدرودینامیکی ناشی از هندسه کانال، طراحی میکروسیال ساده و ابتکاری نیز نشان داده شده است که گرادیانهای غلظت یکبعدی و دوبعدی را با اندازه کوچک تولید مینماید که به طور بالقوه میتواند در کاربردهای میکروسیال PDMS استفاده شود.
در نتیجه، میکروسیالهای PDMS پیشرفتی انقلابی در جستجوی دستگاههای زیست پزشکی مؤثرتر و تشخیصهای نقطهای مراقبت نشان میدهند. مجموعه وسیعی از مطالعات قبل که ابزارهایی را بررسی نمودهاند، به وسیله آنها میتوان خواص فیزیکی و شیمیایی PDMS را برای کاربردهای میکروسیال خاص اصلاح نمود، موقعیت آن را به عنوان ماده انتخابی برتر بیشتر تثبیت مینماید. همانطور که گفته شد، هنوز تعدادی از موانع تکنولوژیکی مانند تکرارپذیری و دوام وجود دارد که مانع اجرای کامل آن در مقیاس تجاری میشود. برای پرداختن به نقش سریع سیستمهای میکروسیال در صنعت زیست پزشکی باید بر این موانع غلبه نمود.
دانلود فایل : استراتژیهای مرسوم و در حال ظهور برای ساخت و عملکرد دستگاههای میکروسیال مبتنیبر PDMS
Reference
Shakeri, A., Khan, S., & Didar, T. F. (2021). Conventional and emerging strategies for the fabrication and functionalization of PDMS-based microfluidic devices. Lab on a Chip, 21(16), 3053-3075.
ترجمه و ویرایش: جواد برزوئی